Согласно примерным программам основного общего образования ФГОС второго поколения деятельность образовательного учреждения в обучении химии должна быть направлена на достижение школьниками личностных, метапредметных и предметных результатов, заданных в виде определенных универсальных учебных действий (УУД).
Остановимся на методических приемах совершенствования у школьников такого УУД, являющегося одним из метапредметных результатов обучения, как использование различных источников для получения химической информации.
Получить химическую информацию на уроках химии учащиеся могут, например, из учебника, фрагментов текстов из источников химического содержания, единой коллекции цифровых образовательных ресурсов (ЦОР).
Рассмотрим некоторые аспекты этого вида деятельности учащихся.
Основной источник информации учащихся – учебник. Одним из видов самостоятельной работы учащихся с текстом учебника является составление плана параграфа. Составление плана служит средством развития умения учащихся логически мыслить. Работа с текстом учебника направлена на формирование умений анализировать изучаемый материал, находить существенное в изучаемом материале и кратко записывать содержание в форме плана, тезисов или конспекта.
В программах школьного курса химии есть несложный теоретический материал, который учащиеся могут усвоить, работая самостоятельно.
Теоретическому материалу, изложенному в параграфе «Вода»[1], предшествует задание для учащихся: «Составьте план параграфа, дав название каждой его части». Несмотря на то, что данное умение учащихся начинают формировать в начальной школе, выполнение заданий, направленных на составление плана, вызывает у школьников определенные трудности. На несложном материале урока раскроем прием совершенствования этого умения.
Напомним учащимся сущность понятия «план», а также функции плана. Планом текста называют выраженную в виде отдельных положений последовательность идей и мыслей, содержащихся в тексте. Правильно составленный план способствует осмысленному усвоению учащимися изучаемой информации, воспроизведению изучаемого материала, т.е. пересказу информации. План используется в качестве организующего начала усвоения учащимися изучаемого материала.
Затем знакомим школьников с «устройством» текста параграфа. Обычно текст разделен на абзацы. Абзац – часть текста от одной красной строки до другой. Он представляет собой одну большую мысль. В учебных текстах эта мысль высказывается в начале абзаца. Далее следует её аргументация.
В параграфе «Вода» разделение текста на абзацы сочетается с нумерацией – числовым обозначением последовательности расположения частей текста. При совершенствовании умения составлять план учащимся необходимо дать названия каждой обозначенной части. Эти названия, перечисленные в последовательности следования абзацев, и будут представлять собой простой план параграфа
Трудность, с которой сталкиваются учащиеся при составлении плана, – нахождение главной мысли в порции материала. Умение выделять главную мысль в части текста лежит в основе формирования умения составлять план текста. Сначала на конкретных фрагментах текста, приведенных в таблице 1 (проецируем на экран или раздаем бумажный вариант), не имеющего отношение к параграфу учебника, но относящегося к теме урока, обучаем школьников умению выделять главную мысль и кратко ее формулировать.
Таблица 1
Составление плана фрагмента текста
|
Фрагменты текста[2] |
План |
|
С формальной точки зрения вода имеет несколько различных корректных химических названий: оксид водорода, гидроксид водорода, монооксид дигидрогена, гидроксильная кислота, англ. hydroxic acid, оксидан (англ. oxidane), дигидромонооксид. |
Химические названия воды |
|
В атмосфере нашей планеты вода находится в виде капель малого размера, в облаках и тумане, а также в виде пара. При конденсации выводится из атмосферы в виде атмосферных осадков (дождь, снег, град, роса). В совокупности жидкая водная оболочка Земли называется гидросферой, а твердая криосферой. Вода является важнейшим веществом всех живых организмов на Земле. |
Нахождение воды в природе |
|
Вода на Земле может существовать в трех основных состояниях – жидком, газообразном и твердом и в свою очередь приобретать самые разные формы, которые зачастую соседствуют друг с другом. Водный пар и облака в небе, морская вода и айсберги, горные ледники и горные реки, водоносные слои в земле. |
Агрегатные состояния и формы воды |
|
Одним из наиболее важных вопросов, связанных с освоением космоса человеком и возможности возникновения жизни на других планетах, является вопрос о наличии воды за пределами Земли… Известно, что некоторые кометы более, чем на 50% состоят из водяного льда… В результате бомбардировки лунного кратера, проведенного 9 октября 2009 года НАСА с использованием космического аппарата LCROSS, впервые были получены достоверные свидетельства наличия на спутнике Земли водяного льда в больших объемах. Жидкая вода, предположительно, имеется под поверхностью некоторых спутников планет, наиболее вероятно, на Титане, спутнике Сатурна, Европе, спутнике Юпитера. |
Наличие воды за пределами Земли |
|
В качестве теплоносителя воду используют в тепловых сетях, для передачи тепла по теплотрассам от производителей тепла к потребителям. Воду в качестве льда используют для охлаждения в системах общественного питания, в медицине. Большинство атомных электростанций используют воду в качестве теплоносителя. В пожаротушении вода зачастую используется не только как охлаждающая жидкость, но и для изоляции от огня в составе пены. Вода используется как инструмент для разрыхления, раскалывания и даже резки пород и материалов. Она используется в добывающей промышленности, горном деле и в производстве. |
Применение воды |
Для формирования умения учащихся находить главную мысль в содержании необходимо систематически возвращаться к работе с текстом учебника или другим источникам информации.
Затем учащиеся приступают к составлению плана изучаемого параграфа.
После того, как названия частей плана составлены и записаны, учащимся необходимо осуществить самоконтроль: прочитать составленный план и решить, помогает ли он вспомнить и воспроизвести содержание текста.
При изучении школьниками 8 класса теоретического материала о воздухе рассматривается материал, известный им из курсов естествознания и ботаники. Поэтому при его изучении можно продолжить совершенствовать умение учащихся находить информацию из учебника. Функции учителя состоят в организации самостоятельной учебно-познавательной деятельности школьников и управлении этим процессом.
Организация самостоятельной работы учащихся с учебником включает следующие этапы: объяснение цели предстоящей работы (целеполагание); формулирование заданий для учащихся; комментирование особенностей их выполнения; проверка выполнения заданий; коррекция знаний и умений учащихся по мере необходимости, оценивание результатов самостоятельной работы.
Учащиеся должны знать, что сформулированные задания будут проверены. В этом случае самостоятельная работа с учебником примет целенаправленный характер.
Целью самостоятельной работы объявляем ознакомление с составом и применением воздуха, выяснением сущности процессов медленного окисления и горения. Для достижения цели необходимо вспомнить из курса биологии о роли зеленых растений на нашей планете, перечислить основные источники загрязнения воздуха, связанные с ними современные экологические проблемы и методы их устранения.
Далее знакомим учащихся с заданиями, которые им необходимо выполнить для достижения целей самостоятельной работы.
Задания для учащихся. №1. Составьте и заполните таблицу, отражающую состав воздуха: укажите название и содержание (в % по объему) постоянных и переменных составных частей воздуха.
№2. Составьте и запишите схему «Применение воздуха».
Подготовьтесь устно ответить на вопросы:
№3. Какие процессы называют медленным окислением, горением»? Приведите примеры такого медленного окисления и горения, которое: а) приносит человеку пользу; б) приносит вред.
Назовите известные вам способы прекращения горения.
№4. Кислород потребляется ежедневно в огромных количествах. Почему его объемная доля в воздухе остается постоянной?
№5. Каковы основные источники загрязнения воздуха? Назовите методы борьбы с загрязнением атмосферы.
Вопросы и задания составлены с учетом задач обучения и планируемых результатов обучения на данном уроке.
Перед каждым видом самостоятельной работы с учебником важен подробный комментарий учителя. Учащиеся, не понявшие цели работы, требований к выполнению заданий, часто обращаются за разъяснением к учителю, нерационально расходуя время. Поэтому, комментируя, обращаем внимание на требования к выполнению заданий. Задания 1 и 2 выполняют письменно, задания 3, 4, 5 – устно; при выполнении заданий 1 и 2 необходимо осуществить перекодирование вербальной информации в таблицу, схему. Указываем источник информации – учебник[3], с. 90-95, а также время, отведенное на выполнение самостоятельной работы с учебником.
Понятно, что все учащиеся работают с разным темпом. Возможно, кто-то из них не успеет выполнить задания за отведенное время. Важно научить школьников быстро находить ответы на задания, рационально использовать отведенное время на выполнение заданий. Это возможно при условии, что разные формы самостоятельной работы школьников на уроке, используя учебник для получения информации, будут организовываться и проводиться учителем систематически.
При организации учебно-познавательной деятельности школьников с источниками информации можно использовать тексты химического содержания. Например, после прочтения такого текста учащиеся должны выполнить предложенное задание.
Задание для учащихся[4]. Прочитайте текст. Составьте формулы оснований, о которых идет речь в тексте.
«Немаловажную роль играют в жизни человека основания. Тысячи тонн гидроксида кальция, или, просто, извести, расходуются на приготовление строительных растворов, штукатурки, хлорной извести. Немало его используется для нейтрализации кислых сточных вод промышленных предприятий, чтобы предотвратить загрязнение окружающей среды…
Гидроксиды натрия, калия и лития в значительных количествах идут на производство соды, поташа, мыла и других соединений. Из них же … приготавливают растворы электролитов для щелочных аккумуляторов… Способность щелочей расправляться с микробами успешно используется, например, при мытье посуды из-под молока, кефира и подобных продуктов. Щелочи к тому же разлагают жир, который удерживает грязь на стенках посуды, и тем самым облегчают мытье…
На основе гидроксидов хрома, марганца, железа, кобальта и меди изготавливают большую часть малярных и художественных красок. А из гидроксида никеля прессуют пластины щелочных аккумуляторов».
(Б. В. Мартыненко «Химия: кислоты и основания»).
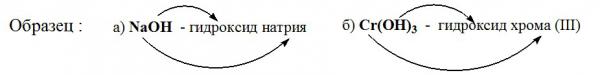
Учащиеся общеобразовательных классов отличаются уровнем усвоения знаний: для кого-то из них сложно воспроизвести информацию, не говоря о том, что знания еще надо уметь применять в разных ситуациях (знакомой или новой) при выполнении заданий. Для мотивации деятельности таких учащихся и создания ситуации успеха при выполнении ими задания можно использовать подсказки и образцы деятельности. Например, для составления учащимися формул оснований, предлагаем «подсказку» и образец действий, приведенные ниже.
«Подсказка»
•Общая формула оснований М(ОН)n
(где «n» = 1, 2 или 3; если «n» = 1, то скобки и индекс не пишутся).
•Общие признаки оснований: 1) сложные вещества; 2) на первом месте в химической формуле атом металла; 3) на втором месте – одна или несколько гидроксогрупп – групп атомов ОН.
• Число гидроксогрупп в основании определяется валентностью металла.
«Образец» действий
Совершенствовать умение учащихся находить химическую информацию можно, используя видеоролики единой коллекции цифровых образовательных ресурсов (ЦОР). Например, информацию этой коллекции можно применять при выполнении учащимися познавательных задач.
Так, изучая химические свойства азотной кислоты (9 класс), можно предложить учащимся посмотреть видеоролик «Взаимодействие безводной азотной кислоты с белым фосфором» (123)[5].
После просмотра видеоролика предлагаем учащимся выполнить задание следующего содержания.
Задание для учащихся. 1) Составьте и запишите схему реакции взаимодействия белого фосфора с безводной азотной кислотой; 2) расставьте коэффициенты в схеме реакции методом электронного баланса; 3) определите окислитель и восстановитель.
Химия – наука экспериментальная. Понятно, что видеоролик не может заменить химический эксперимент. Но в данной ситуации следует учитывать обстоятельство, что белый фосфор - ядовитое вещество, в школьном кабинете химии его нет. Виртуальный мир даёт возможность проводить химический эксперимент без риска для здоровья учащихся и учителя, а также подтвердить истинность теоретического знания.
Изучая свойства концентрированной серной кислоты (9 класс), можно использовать ЦОР для получения учащимися нужной информации, обучая их структурировать изучаемый материал, т.е. составлять структурно-логические схемы. В связи с этим деятельность учащихся следует организовать следующим образом:
просмотр видеоролика (ЦОР) → обсуждение сюжета → выявление элемента структурно-логической схемы.
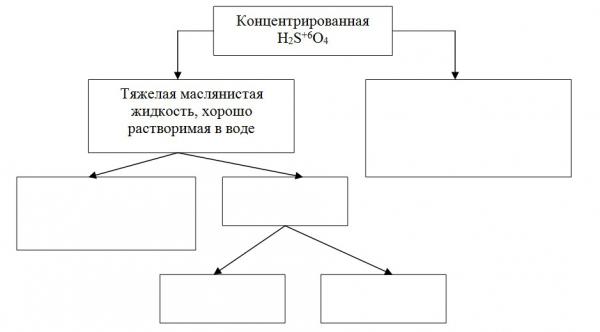
Предложим учащимся «макет» структурно-логической схемы, которую необходимо дополнить недостающей информацией:
Учитель организует деятельность учащихся в соответствии с планом:
1. Просмотр видеоролика[6] 034 «Разбавление серной кислоты».
Обсуждение сюжета.
Вопросы учащимся. Что происходит при растворении концентрированной серной кислоты? Сформулируйте правило разбавления серной кислоты.
Учащиеся заполняют соответствующий элемент схемы.
2. Просмотр видеороликов 032 «Гигроскопичность серной кислоты», 035 «Реакция серной кислоты с органическими веществами».
Учащиеся формулируют наблюдения за химическими явлениями, высказывают суждения, продолжают записывать информацию в схему.
3. Просмотр видеоролика 031 «Взаимодействие серной кислоты с металлами».
Вопросы учащимся. Каковы продукты взаимодействия разбавленной серной кислоты с цинком? Почему медь не вступает в химическую реакцию с разбавленной серной кислотой? Каковы продукты взаимодействия концентрированной серной кислоты с цинком? Медью?
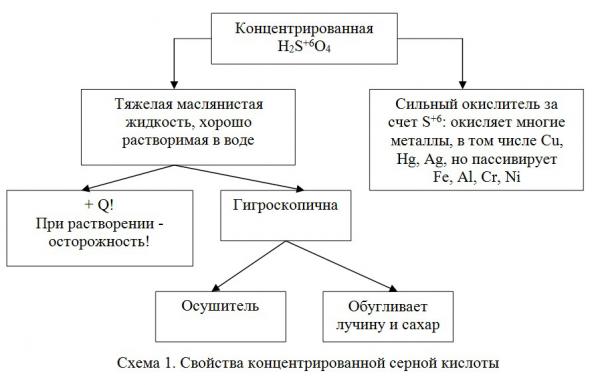
Результат деятельности учащихся – заполненная структурно-логическая схема[7] (схема 1).
Схема 1. Свойства концентрированной серной кислоты
Таким образом, совокупность приемов совершенствования умения учащихся основной школы использовать различные источники для получения химической информации представляет собой общий методический инструментарий учителя. Если различные его формы систематически применять в учебно-воспитательном процессе, то можно наблюдать динамику совершенствования у учащихся этого метапредметного умения.
[1] Е.Е. Минченков и др. Химия. 8 класс. Учебник.
[2] Фрагменты текста взяты на сайте http://ru.wikipedia.org.
[3] Е.Е. Минченков и др. Химия. 8 класс. Учебник.
[4] Химия. 8 класс. Методическое пособие для учителя / Е.Е. Минченков, И.И. Пронина. – М.: Мнемозина, 2013.
[5] Единая коллекция цифровых образовательных ресурсов [Электронный ресурс]: издание официальное. ФГАУ ГНИИ ИТТ Информатика, 2006-2013. URL: http://school-collection.edu.ru/ .
[6] Единая коллекция цифровых образовательных ресурсов [Электронный ресурс]: издание официальное. ФГАУ ГНИИ ИТТ Информатика, 2006-2013. URL: http://school-collection.edu.ru/ .
[7] Химия. 9 класс. Методическое пособие для учителя / Е.Е. Минченков, И.И. Пронина, А.В. Дзенис. – М.: Мнемозина, 2014. – с.250.